有機化合物 〜まずは官能基〜 | 0から始める高校化学まとめ
有機化合物の性質や反応性を理解するためには、官能基の知識が不可欠です。
官能基とは、有機化合物の性質を特徴づける原子や原子団のことであり、同じ官能基を持つ化合物は共通の物理的・化学的性質を示します。
本記事では、炭化水素基と官能基の基本概念を詳しく解説し、以下の内容を学習できます
・炭化水素基とは何か?その種類と特徴
・官能基の構造と性質、及び有機化合物への影響
・代表的な官能基(ヒドロキシ基、カルボキシ基、アミノ基など)の詳細
・有機化合物の分類方法と命名法の基本
これらの知識を身につけることで、有機化合物の理解が深まり、問題解決の力を養うことができます。
はじめにおさえておきたいこと
「アルコール」「お酢」「香水」…実は同じ仲間?
突然ですが、次のものに共通する成分は何でしょう?
お酒(エタノール)
お酢(酢酸)
香水(エステル類)
答えはすべて「官能基」を持つ有機化合物です!
官能基とは、有機化合物の性質や反応性を決定するカギ となる特定の原子団のことです。
例えば、アルコールのヒドロキシ基(-OH) は水とよくなじむため、お酒に溶け込みます。
お酢に含まれるカルボキシ基(-COOH) は酸性の性質を持ち、特有の酸っぱい香りを生みます。
このように 官能基を理解すれば、化合物の性質を予測できる ので、
丸暗記に頼らずに「どんな反応が起こるのか?」を考えられるようになります!
官能基を覚えると何ができる?
化学反応を予測できる!
例:アルコールが酸化するとカルボン酸に変わる
構造式を見て、性質を理解できる!
例:ヒドロキシ基があると水に溶けやすい
高校化学を超えた知識もスムーズに吸収!
大学レベルの有機化学の一部を知ると、むしろ 高校化学の理解が簡単に
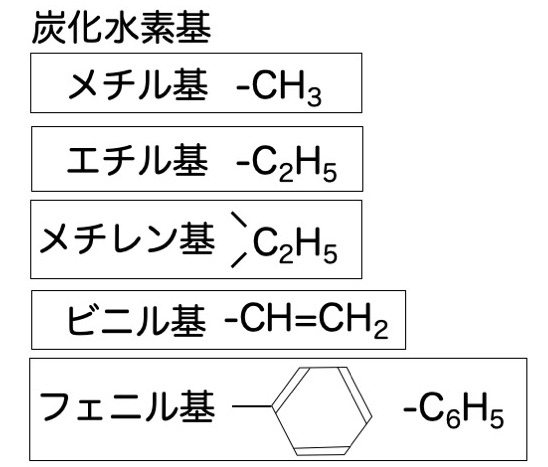
炭化水素基
まず、炭化水素について説明します。炭化水素は、鎖のようになっている鎖式炭化水素、ベンゼンのように環状になっている環状炭化水素に分けられます。さらに、鎖式炭化水素は、飽和炭化水素(アルカン)、不飽和炭化水素(二重結合はアルケン、三重結合はアルキン)に分けられ、環式炭化水素は、脂環式炭化水素(シクロアルカン、シクロアルケン)、芳香族炭化水素に分けられます。
炭化水素を構成している水素原子を、他の原子や原子の集団に置き換えると、様々な有機化合物ができます。この基本となる、「炭化水素から水素原子の一部を除いた原子の集団」を炭化水素基といいます。
炭化水素基は骨格となるものですので、官能基と比べるとそれほど極端な性質は持ちません。おさえるとすれば、電子を渡しやすいか受け取りやすいかなど、結合に関する性質です。
上の図に高校化学でおさえておくべき5つの炭化水素基を示しました。以下でそれぞれの炭化水素基の特徴を解説します。
メチル基
化合物にこのメチル基が結合することを、メチル化と言います。メチル化は生物の体の中で盛んに起きている反応で、アミノ酸、またはDNAやRNAの遺伝情報に関わる核酸と呼ばれる物質もメチル化されることがあります。
構造としては単純な部類に属します。メチル化は求電子付加反応、求核置換反応によって起こる、くらいをおさえておけば高校化学の範囲では問題ないでしょう。
エチル基
エチル基の特徴の一つに、疎水性であることが挙げられます。疎水性とは、水と結びつきにくいこと、水に溶けにくいことを意味しています。
メチル基と共に、電子供与性を示すことが知られています。、
メチレン基
メタンから水素が2つ取り除かれた構造をしています。
高校化学ではメチレン基の名前と構造式を覚えておくだけで問題ありません。コーリー・チャイコフスキー反応などの重要な化学反応に関わりますが、これは専門性の高い道に進んでから学びます。
ビニル基
メチル基、エチル基のように電子供与性を持つのですが、その力はかなり弱くなります。この炭化水素基も、名前と構造を覚えておくだけで問題ありません。
しかし、難関大学の中には、ビニル基が構成要素である酢酸ビニルについて出題するところもごく稀にあるようです。「酢酸ビニルは光や熱ですぐに重合する」を念のために覚えておきましょう。
フェニル基
ベンゼンと似た構造のフェニル基は、有機化学の分野では登場数が非常に多い炭化水素基です。
電子的な性質から見ると、フェニル基はビニル基に似ています。また、フェニル基は疎水性であり、これらの特徴は必ず憶えておかなければなりません。
官能基
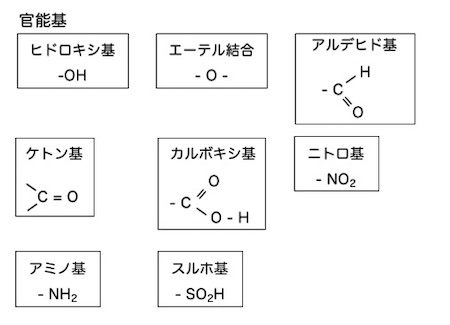
有機化合物の性質を決める最も重要な原子の集団が官能基です。炭化水素基にどんな官能基が結合するかによって、同じ炭化水素基が骨格であっても全く異なる性質を持つ有機化合物ができあがることは少なくありません。
有機化合物の種類は非常に多く、全てを覚えることは不可能と言って良いでしょう。しかし、官能基のどれが結合しているかによって性質が予測しやすくなります。有機化合物の分類は、官能基によって分類されると言っても良いほど、この官能基は重要です。
1つの有機化合物に対して結合している官能基は1つでないこともあり、2つ以上の官能基が1つの有機化合物に結合している場合もあります。こういった場合でも、どれとどれが結合しているか、という組み合わせによって有機化合物の性質が予測できます。
ヒドロキシ基
年齢高めの先生だと「ヒドロキシル基」「水酸基」という人もいます。1価で、弱い酸性を示す官能基です。
「ベンゼン環の水素がヒドロキシ基に置換された化合物はフェノールである。」これはしっかり覚えて下さい。
また、「ベンゼン環以外、例えばアルケン、アルカンなどの水素がヒドロキシ基で置換されると、アルコールになる」これも重要です。
そして絶対に覚えておかなければならないのは、ヒドロキシ基は水素結合によって他の官能基と結合が可能ということです。
エーテル結合
エーテル結合は、複数の化合物の結合を酸素が橋渡しをするような形です。基というより結合形態なのですが、官能基に分類されています。酸素から突き出た2つの手が特徴です。
安定な結合で、ハロゲン化水素、ルイス酸などによって開裂します。開裂とは、共有結合が切断されることを表す言葉です。
エーテル結合を持つ化合物は、エーテルとして分類されます。この化合物は酸素が非共有電子対を持つことが重要な特徴としてあげられます。
環状の炭化水素基をベースとすると、環状エーテルになる事があります。この環状エーテルについては、高校化学の範疇に含める参考書と含めない参考書があるようです。とりあえずは、三員環の環状エーテルをエポキシドと呼ぶ、は暗記しておきましょう。
アルデヒド基
アルデヒド基はホルミル基とも言われ、第一級アルコールを酸化することがよく知られています。炭素と酸素の間の二重結合、そして炭素と水素の結合です。
この基は、タンパク質のアミノ基と反応し、タンパク質を凝固させてしまう働きを持っています。
この基を持っている化合物は、生物にとって有害であることが多く、人間ですと、糖尿病に伴う血管障害や、二日酔いなどに関係します。アルデヒド基を持つ化合物には毒性がある、これは覚えておいて下さい。
ケトン基
ケトン基は、アルデヒド基の水素が外れ、炭素から2つの手が出ている形です。炭素と酸素の二重結合はアルデヒド基と変わりません。
ケトン基はカルボニル基とも呼ばれます。
カルボキシ基
炭素と二重結合する酸素、単結合の酸素、そして単結合の酸素と水素が結合しています。表記のしかたですが、単結合している酸素と水素は、―O―Hと書く場合と、―OHと書く場合があります。
ニトロ基
ニトロ基を持つ化合物をニトロ化合物と言います。ニトロ基が多数結合している化合物は爆発性を持つことがあります。火薬として使われる化合物、トリニトロトルエン(TNT)、ピクリン酸、ニトログリセリンはこのニトロ化合物に分類されます。
ニトロ基を持つニトロ化合物は、鉄を触媒として塩酸と反応してアミンに還元されます。これは暗記しておきましょう。
また、ネフ反応、ヘンリー反応(ニトロアルドール反応)などの重要な反応に関わります。この2つの反応の名前は覚えておいて下さい。反応様式を問うような問題は出ることはほぼないと言えますが、「ニトロ化合物が関わる反応は次のうちどれですか?」という問題が出る可能性はあります。
そのような問題が出題され、選択肢にネフ反応、またはヘンリー反応があっても知らなければ答えようがありません。ぜひともこの2つの反応とニトロ化合物は関係があることを覚えておきましょう。
アミノ基
アミノ基は塩基性の官能基で、酸と塩を作ることが知られています。アンモニア、NH3から水素が一つはずれた形ですので覚えやすい官能基です。
アミノ基には2つの水素原子があります。この水素原子が別の官能基と結合し、官能基のアミノ基に別の官能基が結合する、という事も起こります。
注意する事としては、アミノ基は塩基性を示すのですが、ホルムアミドなどの酸アミドはアミノ基を含むにも関わらず中性を示します。
スルホ基
炭素骨格にスルホ基が結合すると、一般名がスルホン酸という化合物になります。スルホン酸には、塩化スルホン酸、フルオロスルホン酸など多数の化合物があります。
スルホ基は高校化学で習う官能基の中で、唯一、硫黄(S)を含みます。スルホ基の特徴は、強酸性と強い電子求引性です。そして親水性であり、水と良く水和します。
基の考え方
化学には基という概念があり、それによって性質が予測できたり、名前が変わったりします。基本的な3つの基は置換基、特性基、そしてここで解説した官能基です。
これらの使い分けは高校化学の範囲ではありません。また、基の概念もそれほどきっちりしたものではなく、新しい考え方や発見によって変化しています。そのため、高校化学では基についての概念は学ばずに、“官能基”を学びます。官能基は他の2つ、特性基、置換基と比べると概念が明確だからです。
しかし高校化学で置換という言葉は出てきますし、官能基を考えるときに便利なのでここで解説します。
置換基
置換基は、化合物の種類などを決定する時に重要となるもので、化合物の名前の付け方にも影響します。
有機化合物は分類可能であり、母体となる化合物ごとに分けることができます。同じカテゴリーに属する化合物は、当然構成する原子が異なる部分があります。
共通する部分は、母体と呼ばれることが多いのですが、親化合物という表現も使います。そして同じカテゴリーでも異なる部分が置換基と呼ばれます。
特性基
化合物の特徴を決めるために必要な基です。この特徴は、性質などよりもむしろ見た目、形式的な意味合いを持つ事がほとんどです。
この記事で扱った官能基は、この特性基の集合体(特性基1つでも官能基が成立する場合があります)によって構成されたものといえます。
例を挙げますと、ケトン基(カルボニル基)がわかりやすいです。
ケトン基は、炭素鎖のメチレン(―CH2―)に、特性基であるオキソ基(=O)が結合したものです。つまり、
メチレン(炭素鎖)+ オキソ基(特性基)= ケトン基
となっているのです。
構造式で化合物の端っこにおることが多いので、特性基について考えなければならないときにはまずそこに着目して下さい。
官能基
化合物の物質としての属性、化学的に着目した場合の性質など、化学反応に重要なものです。現代では置換基と同じ意味として使われる事もあり、その定義は曖昧になっています。
この官能基によって化合物には化学的特性と、物性が与えられます。物性とは、物質の物理的性質のことで、力学的な特徴、熱を加えるとどうなるか冷やすとどうなるか、電気に対してはどうか、電導性があるのか、その他にも磁気についてなどの性質を示します。
この物性は化学的反応に大きく影響しますので、官能基の付加による物性の変化を理解することは、有機化学の理解に非常に重要です。
官能基による化合物群の名称
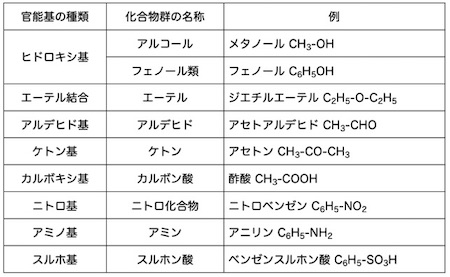
官能基によって決められた化合物の性質は、そのまま化合物の分類につながります。上の図に官能基による化合物群の名前を示しました。
これらは暗記が必須です、必ず覚えて下さい。
そして頻出ポイントは、ヒドロキシ基がどうなるとアルコールになって、どうなるとフェノールになるか?です。
これは解説しましたが念のためにここにも書いておきます。必ず覚えて下さい。
・ベンゼン環の水素がヒドロキシ基に置換された化合物はフェノールである。
・ベンゼン環以外、例えばアルケン、アルカンなどの水素がヒドロキシ基で置換されると、アルコールになる。
そして代表的な化合物を表に具体的に挙げてあります。これらも暗記して下さい。できれば1つではなく、数個調べて暗記しておくと便利です。
ノートや裏紙に構造を何度も書いて、しっかり頭に入れましょう。最後の表に挙げた代表的な化合物も書いて覚えましょう。
ここを理解できると、試験で大きな得点ポイントになります。しっかり学習しましょう。



