1. 化学を攻略するためには単位の理解が必須
化学の計算問題のほとんどには単位がついてきます。
問題文の中の単位を、解答するときには別の単位に変換しなければならなかったりすることが多く、これが理由で化学の計算問題は苦手という方は多いのではないでしょうか。
さらに、高校化学では「モル」という厄介な単位があります。
化学の単位変換には、いくつかの種類があります。まずは単位変換のパターンを紹介し、その後に勉強方法を解説します。
1.1. 接頭語を使った単位変換
接頭語、と書くと難しそうに思えますが、普通に我々が使っているものです。
ギガ、メガ、などは数量を表す接頭語です。このギガ、メガの仲間が高校化学では出てきます。
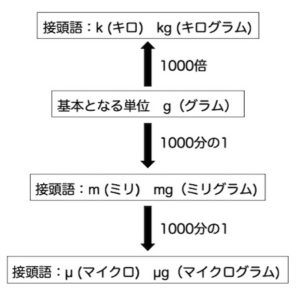
1グラムの1000倍、1000グラムは1キログラム(1 kg)に変換されます。このk (キロ)が接頭語と呼ばれるものです。
メートルの1000倍であれば、キロがついて1キロメートル(1 km)です。皆さん、普通に使っていますよね?
ちなみに、キロの1000倍がメガ(M:大文字で使います)、メガの1000倍がギガ(G:これも大文字で使います)です。
それでは1000分の1になるとどうなるでしょうか?
1グラムの1000分の1は、1ミリグラム(1 mg)となります。このm(ミリ)が接頭語になります。
長さの単位ですと、メートル(m) → センチメートル(cm) → ミリメートル(mm)となります。センチメートルを挟んでいるのでちょっとややこしいですが、1メートルの1000分の1は、接頭語のm(ミリ)を付けて1 ミリメートル(1 mm)になります。
化学であれば、ミリの1000分の1も押さえておきましょう。ミリの1000分の1は、マイクロ(µ)という接頭語を使います。
1.2. 文字が完全に変わる単位変換
接頭語を使った単位変換ですと、グラム → ミリグラム → マイクログラムで覚えやすいのですが、文字が完全に変わってしまうのはちょっとやっかいです。
例を挙げると、立方センチメートル(cm3 )からリットル(Lまたはl)への変換です。
1リットルは1000立方センチメートル(1000 cm3)です。10センチメートル x 10センチメートル x 10センチメートルの容器が1リットルとなります。
長さを表す単位では、1オングストローム(1A)は0.1ナノメートル(0.1nm)が代表的です。ちなみに、ナノメートルのナノは、マイクロの1000分の1です。
1.3. 数字が変わる単位変換
文字が変わるだけならともかく、数字も変わる単位変換もあります。
例えば、熱量、エネルギーの単位であるジュール(J)は、1 ジュール(1 J) = 0.24カロリー(0.24 cal)です。逆に1カロリーは4.18ジュールです。
圧力ですと、パスカル(Pa)という単位がよく出てきます。1パスカル(1 Pa)を別の単位に変換すると、 9.87 × 10-6 アトム(9.87 × 10-6 atm)または、7.50 × 10-3 mmHg(ミリメートルエッチジーと読みます)です。mmHgは、水銀柱ミリメートルとも言われます。
1.4. 勘違いが意外と多い、体積の変換
体積、容積の単位の変換は、勘違いによる間違いが多く見られるところです。
どういう勘違いかといいますと、1メートル(1 m)は100センチメートル(100 cm)であることから、1立方メートル(1 m3)を100立方センチメートルにしてしまう間違いがよく見られるのです。
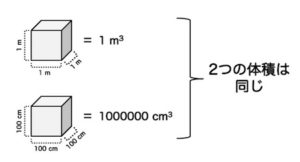
タテ、ヨコ、高さが、1メートル x 1メートル x 1メートルの入れものが1立方メートルの体積です。
これをセンチメートルに変換すると、100センチメートル x 100センチメートル x 100センチメートルの入れものが1立方メートルとすることができます。
では、1立方メートルを立方センチメートルに変換するとどうなるかですが、100センチメートル x 100センチメートル x 100センチメートルなので、1000000立方センチメートル、つまり、1立方メートル(1 m3) = 1000000立方センチメートル(1000000 cm3)になります。
長さを表す単位のパターンは体積・容積の単位変換に使えない、ということを頭の中にきちんと入れましょう。
1.5. 単位のラスボス的存在のモル
高校化学の単位変換で最も混乱するのはモルです。モルという単位は、長さなのか体積なのかはっきりしませんので想像しにくいですよね。
モルは「物質量」というものの単位です。
物質量とは何か?という話を始めると、大学で勉強する範囲が必要になってしまいます。
しかも、一昔前は「物質量=モル数」と言われていましたが、現在は同じとしてはいけないとされています。
科学の進歩によって概念が変わったりすると、今まで認められていなかったものが認められたり、今まで正しかったものが正しくないとされたりします。
ですので、ここはひとまず「物質量を考えたり、物質同士を比較するときに都合のよい単位」くらいで頭に入れておきましょう。
実際、理工系、医療系の大学に進学すると、このモルという単位はよく使います。
非常に便利で使いやすく、研究などでは物質の濃度を比較したり理解するにはなくてはならない単位です。使いこなせれば、高校の勉強、大学受験だけでなく、大学進学後も重宝します。
1.6. 単位を使わないものもある
単位は重要ですが、化学には単位をつけてはならない数値も出てきます。
それは、原子量、分子量です。この値は相対値なので、無次元量と呼ばれており、単位をつけないことになっています。
相対値には基本的に単位はつきません。偏差値はその代表的な数値です。
2. 単位変換とモル計算の勉強方法
単位変換とモル計算の攻略方法は、「暗記」と「訓練」です。
この分野は、勉強した量がそのまま点数に直結する分野です。勉強すればするほど高得点が期待できます。
しかし、手順を間違えると、時間をかけている割に理解するスピードが遅く、イライラして手につかなくなってしまいます。
勉強方法にはそれぞれの人に適したやり方はありますが、ここでは、化学の単位変換の能力を基礎からしっかり作り上げたい人向けの勉強方法を解説します。
2.1. 暗記することを整理する
まずは、高校で出てくる単位をまとめたものを作りましょう。
ノートと言いたいところですが、それほどページ数は必要ではないので、ルーズリーフにまとめてもいいと思います。
できれば、1ページに全部まとめられると暗記の時に楽です。
きれいに書くことが目的のまとめノートは無駄ですが、この場合は「単位の辞書」を作ることが目的です。
参考書、教科書にまとめて掲載されていることもあります。もしそれがあれば自分でまとめる必要はありません。そのページに付箋を貼るなどして、すぐに出せるようにしておきましょう。
2.2. 暗記するために問題集を解く
まずはそのまとめられたものを暗記してから問題を解きたくなりますが、すぐに問題を解き始めましょう。
化学の計算問題をまとめた問題集が普通に販売されていますので、まずは薄い問題集、つまりはページ数が少ない問題集を選んで下さい。
あまり厚めの問題集ですと終わらせるまでに時間がかかります。単位変換の勉強は、暗記と訓練というまり楽しくない作業ですので、やり切った感でモチベーションを保つためにも、すぐに終わらせられそうな薄い問題集を選んで下さい。
その問題集を、単位変換がまとめられたものを見ながら解いて下さい。問題を解いているうちに、まとめられた内容が頭の中にインプットされます。
これは、まとめたものを見ながら暗記するよりも、実際に解いたほうが暗記しやすいからです。
単位変換に特化した問題集があれば最適です。そんな問題集を見つけたらすぐに買いましょう。
2.3. 暗記の確認のために問題集を解く
頭に入ったかな、と感じたら、次はまとめたものを見ずに解いてみましょう。頭に入っていなくても気にする必要はありません。まとめたものをもう一度見ればいいだけの話です。
まとめたものを見なくても解ける問題が必ずあるはずですが、そういう問題が少ないからといって、前に戻る必要はありません。
まとめを見ずに解いて、忘れていたらまとめをもう一度見る、これでやり切りましょう。
ここで大事なポイントの一つは、解いた過程、計算の過程を必ずどこかに書き残すということです。
間違えたときに、ただ間違えたではなく、解いた過程を見てどこを間違えたのかを把握することが実力アップの近道です。
2.4. 単位変換だけなくパターンも頭に入っているはず
ここまでやると、単位変換が頭に入っているだけではなく、計算問題のパターン、解き方のパターンも頭に入ってきます。
問題がどう出題されるか?どこから手を付けるのか?というパターンがだいぶ身についているので、仕上げにもう一冊問題集をやれば、計算を使った総合的な問題にチャレンジする準備は完了です。
大学入試の問題は多かれ少なかれ、あるパターンに沿って出題されます。化学という学問の中で、高校までに履修する範囲はそれほど広くないので、どうしても出題する問題がパターン化されてしまうのです。
単位変換の問題に関しては、ここまでやり切れば、かなりの数のパターンに対応できる力が身についています。
この後、時々は計算問題に戻って実力を維持すれば、単位変換の問題はそれほど怖くなくなります。
2.5. モル計算の勉強方法
長さや体積、熱量という具体的にイメージできる事柄を表現する単位と違って、モルはどんな単位なのかなかなか想像が難しい単位です。
そのため、勉強するときにどう手をつけていいのか悩む方も多いかと思います。
モルについて勉強するときには、まずモルとアボガドロ定数の関係から手をつけます。
物質量などの言葉がこの辺では出てきます。しかし、いったん物質量は脇に置いて、モルとアボガドロ定数の関係をしっかりと頭に入れましょう。
酸素でも水素でも、あらゆる物質は、1モルの中に、6.02 x 1023個の分子があります。
6.02 x 1023という数字をアボガドロ定数といいます。
「6.02 x 1023 はアボガドロ定数という」これをしっかり頭に入れて下さい。
1モルとアボガドロ定数の関係の次に、さっき脇によけた物質量の関係を勉強しましょう。この時の仕上げには、いろいろな物質を選んで、「1モルは何グラムか」と「1モルの分子数はいくつか」を考えます。
アボガドロ定数と1モルの関係が理解できたら、原子量、分子量とアボガドロ定数、1モルの関係について、教科書などの文章を使って理解しましょう。
炭素、酸素などの原子、二酸化炭素などの分子を使ってグラムと分子数を答えられるようになり、アボガドロ定数、モル、原子量または分子量の関係を紙にスラスラ書けるようになればクリアです。
2.6. モル計算の問題はただの計算問題ではない
モルを使った計算問題は、先の述べた長さや体積の単位とはちょっと違う雰囲気です。
覚えていることを試すような問題よりも、解答までのプロセスを試す問題が多く出題されます。
ですので、問題集などを解いたときには、解答の過程はきっちりノートに書きましょう。
勉強しているときに気をつけなければならないのは、モルの計算問題は、計算間違いよりも考え方の間違いを気にした方が実力アップにつながります。
3. まとめ
単位変換で暗記しなければならないことは、何問も解いているうちに頭に入ります。最初に完全暗記する方法もありますが、ほどほどに暗記できたら実際の問題を解いてみる方が、得点力アップは早いと思います。
そして化学の計算問題では、最終的に出した答えが正しいか正しくないかを気にしがちです。
問題集を解いているときに、途中のプロセスを書き留めずに解答し、正解かどうか答え合わせをする、という勉強方法では、なかなか化学の実力は上がりません。
化学の単位変換を含む問題、モルを使った計算問題では、計算の途中のプロセスをしっかり書きながら解いて下さい。
間違えたら、解答の間違いよりも計算プロセスのどこを間違えたのかをチェックして下さい。
プロセスの間違いは、すぐに修正して同じような問題を数問続けて解くと、同じ間違いをしにくくなります。
化学の計算問題は苦手な人が多いので、こなせるようになると受験で有利です。
まずは手をつけてみましょう。勉強量が素直に実力に直結するので手応えがはっきりとわかります。