元素 〜重要な元素の性質〜 | 0から始める高校化学まとめ
化合物の性質、反応を知る上で、元素それぞれの性質を知っておくことは重要です。この記事では、知っておくべき元素の性質について解説します。

この記事では、重要な元素のうち、典型元素に属するものの性質について解説します。化合物の反応、性質を理解するためには、その化合物の元素の性質を知っておくことが重要です。
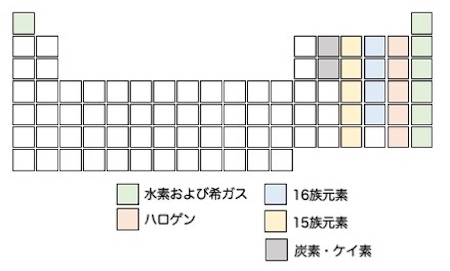
扱う元素の周期表における位置は、上の図に示しました。元素の性質と共に、それぞれの代表的な化合物についても解説します。
水素・希ガス
水素・希ガスに分類される元素は、水素(H)、ヘリウム(He)、ネオン(Ne)、アルゴン(Ar)、クリプトン(Kr)、キセノン(Xe)、ラドン(Rn)です。
水素(H)は、単体の時には2分子、H2/sub>で存在します。無色・無臭の最も軽い気体であり、水に溶けにくいという性質を持っています。
水素の製法は、代表的な3つの方法を覚えておきましょう。
・コークスに水蒸気を送り込み、炭素 + 水 → 一酸化炭素 + 水素の反応で水素を取り出す。
・水を電気分解する。
・天然ガス、ナフサをニッケルなどの触媒を使って水蒸気と反応させて水素を取り出す。
水素は水に溶けにくいので、集めるときには水上置換によって捕集することができます。また、水素を高温にすると、強い還元作用を示しますので、還元剤として使われる事もあります。
希ガスは原子が単独で安定です。そのため、空気中では単原子分子として存在します。融点・沸点が非常に低いため、常温では気体です。この性質を使って、冷却剤として使われます。
また、放電管にこれらの気体を封入して放電すると、元素それぞれ特有の発色をします。例えば、ネオンの場合は赤を発色します。ネオンサインという言葉はここからきています。
ハロゲンに分類される元素

ハロゲンに分類される元素は、フッ素(F)、塩素(Cl)、臭素(Br)、ヨウ素(I)、アスタチン(At)です。
ハロゲン単体の性質
ハロゲン元素は有色、つまり色がついています。そして、全て2つの原子から形成されています。つまり、F22の状態で存在しています。
これらは強い酸化力を持ち、有毒です。酸化力の強さは、原子番号が小さい元素ほど強いことは必ず覚えておきましょう。
元素ごとの性質を見ていきます。まずは塩素です。塩素は製法も頻出ですので覚えて下さい。
塩素は工業的には食塩水を電気分解して生産されています。また、二酸化マンガンに濃塩酸を加えて加熱、塩化ナトリウムに濃硫酸、二酸化マンガンを加えて加熱することによっても生成できます。
塩素は黄緑色で刺激臭があります。強い酸化作用を持つことから、漂白剤、殺菌剤として利用されています。さらに、塩素は科学的に化合物を作りやすく、多くの元素と直接化合することによって塩化物を作ります。
臭素は赤褐色です。液体だけでなく気体も赤褐色で、刺激臭があり有毒です。特徴的な性質は水より重いことです。水にはわずかしか溶けません。
ヨウ素は、常温の状態では黒紫です。さらに板状の結晶で一見すると金属のような感じです。ヨウ素には昇華性があるので、熱すると固体から直接気体になります。冷却すると、液体を経由せずに固体に戻ります。
ヨウ素は水にはほとんど溶けませんが、有機溶媒によって溶かすことができます。このヨウ素を含む溶液に、デンプンを含んだ水溶液を混ぜると、ヨウ素デンプン反応によって溶液は青くなります。
フッ素は常温で淡い黄色を示します。刺激臭があり、有毒です。他のハロゲンと比べてかなり強い毒性を持っています。
ハロゲン化水素
ハロゲンは水素と化合がしやすく、ハロゲン化水素を形成します。
よく出題されるハロゲン化水素は、フッ化水素(HF)、塩化水素(HCl)、臭化水素(HBr)、ヨウ化水素(HBr)です。ここに挙げたハロゲン化水素は全て常温では無色の気体として存在し、刺激臭があります。
フッ化水素は弱酸を示し、他の3種類のハロゲン化水素は強酸を示します。ここは非常に重要なので必ず覚えて下さい。性質については、塩化水素の水に非常に溶けやすく、溶けると塩酸になり強い酸性を示すことと、フッ化水素の水に非常に溶けやすく、溶けると弱酸性を示すことは重要事項です。
ハロゲン化水素では製法がよく出題されます。塩化水素とフッ化水素の製法が出題のほとんどを占めます。
塩化水素は、工業的製法では食塩水を分解し、得られた水素と塩素を直接化合させて作ります。また、塩化ナトリウムに濃硫酸を加えて加熱する方法は、揮発性の酸の塩に不揮発性の酸を加えて熱を与えると、揮発性の酸が出る反応の代表例です。
フッ化水素は、フッ化カルシウム(蛍石ともいう)に濃硫酸を加えて加熱します。この反応も、塩化水素と同じく揮発性の酸の塩に不揮発性の酸を加えて熱を与えると、揮発性の酸が出る反応の代表例です。
ハロゲン化銀、オキソ酸
ハロゲンと銀の反応は非常に重要です。ハロゲンのうち、塩素イオン、臭素イオン、ヨウ素イオンのいずれかが含まれている水溶液に、硝酸銀を加えると沈殿が生じます。この沈殿はそれぞれ、塩化銀、臭化銀、ヨウ化銀です。ただし、フッ素も反応はするのですが、生成するフッ化銀は水に溶けやすいので沈殿にはなりません。
ここで生成したハロゲン化銀は光に反応する感光性があります。塩化銀は白色、臭化銀は淡い黄色、ヨウ化銀は黄色ですが、日光に当てると、塩化銀、臭化銀、ヨウ化銀は、銀が遊離して黒くなります。
ハロゲンを含むオキソ酸は、特に塩素を中心に学習しましょう。
塩素からできるオキソ酸は、酸性度の強い順に、過塩素酸、塩素酸、亜塩素酸、次亜塩素酸となります。酸性度が最も低い次亜塩素酸が最も酸化力が強い化合物になります。
16族元素
単体での性質など
ここで学ぶ元素は、酸素(O)、硫黄(S)、セレン(Se)、テルル(Te)です。これらは非金属元素で、酸素族元素という呼び方もあります。
16族元素にが関係する問題には、「どこに存在するか?」が重要で、問題によく出されます。
酸素は、酸化物として、または塩で地殻に多く存在します。硫黄は黄鉄鉱、黄銅鉱、セン亜鉛鉱、方鉛鉱として地殻中に存在します。セレンとテルルは、酸素、硫黄と比べると量は少なく、硫黄と一緒に見つかる元素です。
この4つの元素のうち、特に重要な元素は酸素と硫黄です。酸素についてはその製法、硫黄は同素体についてが問われます。
酸素の製法は、水の電気分解、過酸化水素水と酸化マンガンを反応させる、塩素酸カリウムに酸化マンガンを加えて加熱する、を覚えておけば大丈夫です。性質は、無色・無臭で水に溶けにくいこと、オゾン(O3)になると、淡い青色を示し、不安定になる、オゾンはヨウ化カリウムデンプン紙を青くする、はしっかり覚えておきましょう。
硫黄には、斜方硫黄、単斜硫黄、ゴム状硫黄という同素体があります。区別は、斜方硫黄が黄色、単斜硫黄が淡い黄色、ゴム状硫黄が褐色をしています。性質は、斜方硫黄が最も安定で、単斜硫黄は95.5℃から455℃まで安定です。ゴム状硫黄は不安定で、斜方硫黄に変化してしまいます。
これら硫黄は水には溶けません。斜方硫黄と単斜硫黄は二硫化炭素に溶けます。
16族元素の水素化合物
16族元素の水素化合物には、酸素の水素化合物である水、硫化水素、セレン化水素、テルル化水素があります。水以外の水素化合物は、常温において無色・有毒の気体です。においも特徴的で、硫化水素とセレン化水素は卵が腐ったような独特のにおいがします。
水、硫化水素、セレン化水素の沸点と融点を比べると、融点は水が0℃、硫化水素が-85.5℃、セレン化水素が-65.7℃、沸点が水は100℃、硫化水素-60.7℃、セレン化水素は-42℃です。水は最も分子量が小さいのですが、他の水素化合物と比べて沸点、融点が非常に高くなっています。これは、水分子は、分子間に水素結合が形成されているためです。
水は極めて安定な物質です。分子間の水素結合と、固体、つまり氷になると体積が液体の時より大きくなるのが特徴です。
水に酸素が1分子付加すると、過酸化水素になります。過酸化物は化合物内に、
H-O-O-Hという酸素原子同士の結合を持ちます。一般的に性質は不安定とされています。
16族元素の化学反応における重要なポイントとして、硫化水素と金属イオンによる沈殿の生成があります。水溶液中の硫化水素は弱酸性を示し、金属イオンと反応することによって、金属硫化物の沈殿を生じます。
16元素の酸化物とオキソ酸
二酸化硫黄、硫化水素がここでは重要です。二酸化硫黄は無色で刺激臭がある有毒な気体、
硫酸は、濃硫酸の時には無色で粘性のある気体です。不揮発性ですので、揮発性の酸からできた塩に加えて熱を与えると、揮発性の酸を発生します。希硫酸は強酸性の酸化力がない液体で、イオン化傾向が水素よりも大きい金属と反応すると水素を発生します。
ここで絶対に覚えておきたいのは、濃硫酸は不揮発性、脱水性で、加熱すると酸化力が強くなる。希硫酸は強い酸性を示し、酸化力、脱水性はなく、種々の金属を溶かす性質を持っていることです。
15族元素
15族元素は窒素族元素ともいわれ、窒素(N)、リン(P)、ヒ素(As)、アンチモン(Sb)、ビスマス(Bi)です。
単体の性質
単体の性質で押さえておかなければならないのは窒素とリンです。
窒素は分子の状態で存在し、大気の78〜80%を占めていて、常温では安定です。天然に存在する窒素の多くは、生物の体の中にアミノ酸、タンパク質の一部として存在しています。
リンも同様に、生物の体の中に存在しています。主に、リン脂質、DNA、RNAなどの核酸の構成元素として存在しています。
窒素は無色・無臭の気体で水に溶けにくく、常温では化学変化を起こしにくい元素です。しかし、高温になると、一酸化窒素、二酸化窒素などの窒素酸化物を作ります。
リンには、黄リンと赤リンという同素体が存在します。 黄リンは反応性が強く、有毒です。空気中では自然発火する元素のため、水中で保存されます。赤リンは常温では安定です。
窒素、リンの化合物
窒素の化合物でぜひ覚えておかなければならないのはアンモニアです。アンモニアは窒素と水素を鉄を触媒にして直接反応すると得られます。この方法はドイツの科学者ハーバーによって考案され、ハーバー・ボッシュ法と言われています。
アンモニアは水に非常に溶けやすく、水溶液は弱い塩基性を示します。アンモニアイオンはネスラー試薬で検出することができ、アンモニアイオン存在下では、黄褐色、赤褐色の沈殿を生じます。
このアンモニアは酸化させることによって、一酸化窒素、そして一酸化窒素を酸化させると二酸化窒素が合成されます。これはオストワルト法というアンモニアの酸化方法です。この方法で合成される一酸化窒素は、無色・無臭の気体、二酸化窒素は赤褐色の有毒な気体です。
オストワルト法は最終的に二酸化窒素から硝酸を得る方法です。バーバー・ボッシュ法とオストワルト法は、近代産業の成立に重要な役割を果たした方法ですので、必ず覚えて下さい。
得られた硝酸は、濃硝酸と希硝酸があります。どちらも酸化力があり、銅、銀を溶かすことのできる液体です。
リンの化合物で重要な物質は、十酸化四リンです。P4O10と書いた方がわかりやすいでしょう。この物質は吸湿性が強く、乾燥剤、脱水剤として使われています。
また、リンの化合物である過リン酸石灰は、農業において重要な肥料として使われています。リンも窒素も、生体中に存在するため、肥料として使われている重要な元素です。
炭素・ケイ素
単体での性質
炭素(C)、ケイ素(Si)は14族元素に含まれます。これらは炭素族元素と言われます。顕著な特徴として、これらの原子は4個の価電子を持っており、共有結合の化合物を作ります。
炭素は天然に多量に存在します。ダイヤモンド、黒鉛(グラファイト)などの同素体があり、最近ではフラーレン、カーボンナノチューブが発見されました。結晶化されていない炭素は木炭に代表される炭です。
炭素の同素体は、黒鉛であれば電気を通しますが、ダイヤモンド、フラーレンは電気を通しません。また、黒鉛は柔らかい結晶ですが、ダイヤモンドは極めて硬い結晶です。
ケイ素は、灰色の金属のような光沢を持ちます。共有結合の結晶で、非常に堅い結晶です。金属と絶縁体の中間の電気伝導性を示し、半導体と呼ばれます。
炭素・ケイ素の化合物
炭素の化合物で最も重要なのは、二酸化炭素です。
二酸化炭素は、無色・無臭で空気より重く、酸性酸化物の性質を持ちます。酸性酸化物ですので、塩基と反応して塩を作ります。
また、石灰水に二酸化炭素を吹き込むと石灰水が白く濁ります。そしてさらに吹き込むと透明になる、という性質はしっかり覚えておきましょう。
炭酸塩は弱酸性の塩で、強酸と反応して二酸化炭素が発生します。また、炭酸イオンは、塩化カルシウム水溶液を加えると白色沈殿を生じます。
二酸化ケイ素はケイ素の化合物の中で最も有名な化合物です。シリカとも呼ばれ、巨大で安定な物質です。水晶、石英などで天然に存在し、工業的にも重要で、セメントなどの原料になっています。
特に沈殿反応は重要です。どういう性質の時に沈殿が生じるのか、沈殿を生じる化合物の組み合わせはどれか、は非常に重要です。
各元素の特徴を、色・におい、水に溶けやすいか溶けにくいかなどに着目してしっかり学習しましょう。




